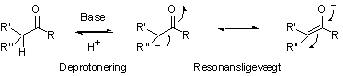5: Syre-base kemi, resonansstabiliseringSvage syrer og enormt stærke baserTeori-del Nogle strukturer kan opskrives på flere former, der kun adskiller sig ved, at elektronerne er forskelligt fordelt. Sådanne former kaldes resonansformer. Et stof eller en gruppe, der kan optræde på flere resonansformer, er særlig stabil, fordi elektronerne er spredt mere ud (delokaliseret) over stoffet/gruppen. Sådanne former siges at være i resonans med hinanden. Krumme pile er gode til at vise, hvorledes et stofs resonansformer kan overføres til hinanden.
Opgave 5.1
Teori-del Hvis en protonfraspaltning giver anledning til dannelse af en resonansstabiliseret anion vil protonfraspaltningen favoriseres, og syrestyrken øges. Hydrogenatomer på C-atomer ved siden af carbonylgrupper er (meget svagt) sure (pKs = 20). Dette skyldes, at fraspaltning af en proton giver en anion, der er relativt stabil, fordi dens negative ladning kan fordeles på (delokaliseres over) to atomer. Dette ses ved at bruge krumme pile til at vise, hvordan den negative ladnings elektronpar kan flytte sig fra C til O og tilbage igen.
Protoner på C ved siden af C=O er (meget svagt) sure og kan fraspaltes ved hjælp af stærk base
Opgave 5.2
Hint: Analysen kræver opskrivning af resonansformerne for den carbanion, der dannes, når ethylpropanoat deprotoneres.
Opgave 5.3
Opgave 5.4
Opgave 5.5
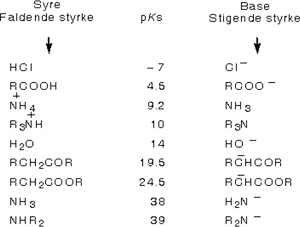
Teori-del Ammoniak, primære aminer og sekundære aminer kan både kan optræde både som baser og som syrer. Syreregenskaberne er yderst svage ifølge pKs-værdien, der fx for NH3 er 38. Derfor er de korresponderende baser enormt stærke.
Opgave 5.6
pKs værdier for udvalgte syrer. |