Emulgatorer - hvorfor er de nødvendige?
Hvilke væsker kan blandes?
Olivenolie er ikke blandbart med vand, derimod kan ethanol blandes med vand i alle forhold. Hvis vi skal forstå, hvorfor det forholder sig sådan, må vi se nærmere på opbygningen af vandmolekylet og molekylerne i fedtstoffer eller spiseolier.
 |
 |
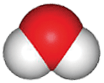
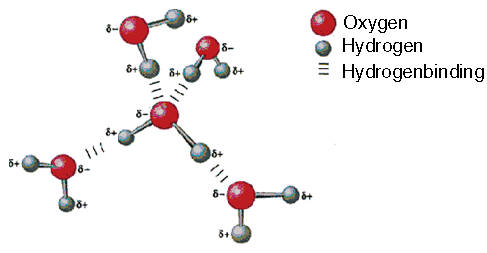
Mellem O-atomet og hvert H-atom er der en elektron-parbinding (kovalent binding). Det fælles elektronpar, som udgør en enkeltbinding i molekylet, fordeles ikke ligeligt mellem O- og H-atomet. Oxygenatomet trækker mere end hydrogenatomet i det fælles elektronpar mellem de to atomer. Herved bliver en større del af den fælles elektronsky trukket over mod oxygenatomet. Da elektronskyen er negativ, får O-atomet et lille overskud af negativ ladning, d - (delta minus). H-atomet mister derimod en del af det fælles elektronpar og bliver svagt positivt ladet, d+ (delta plus).
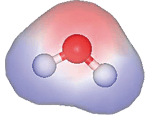
Oxygensiden af vandmolekylet er negativ, og et punkt midt mellem H-atomerne er center for en svag positiv ladning. Da centeret for positiv og negativ ladning i molekylet ikke er sammenfaldende, er molekylet polært.
Da vandmolekyler er polære og samtidig små, kan hydrogenatomet i et vandmolekyle tiltrække elektroner fra et O-atom i et nabomolekyle. Derved kommer hydrogenatomet til at danne bindinger mellem vandmolekylerne. Disse bindinger kaldes hydrogenbindinger. Da vandmolekylet er et polært molekyle, kaldes vand et polært opløsningsmiddel.
 |
 |
 |
 |
Andre molekyler, fx alkoholer, indeholder også et hydrogenatom, der er bundet til et oxygenatom, altså atomgruppen -OH. Grupper, der ligesom -OH kan danne hydrogenbindinger, kaldes hydrofile grupper.
Emulgatorer - hoved og hale
En emulgator gør det muligt at blande et polært stof med et upolært stof, fx olie og eddike til en salatdressing. Et emulgatormolekyle skal altså forene egenskaber fra et polært og et upolært molekyle. Det gør monoglycerider.
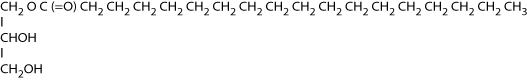

I et monoglycerid sidder der kun en fedtsyreenhed på glycerolskelettet, se figuren.
Et emulgatormolekyle kan illustreres meget forenklet som en hydrofil kugle på en hydrofob pind (eller hale).
![]()
Det hydrofile hoved bindes til vand med hydrogenbindinger, mens den hydrofobe hale danner svage bindinger til upolære molekyler.
Når vi opløser en smule emulgator i vand, vil emulgatormolekylerne nær vandoverfladen anbringe sig med den hydrofile del nede i vand og den hydrofobe del stikkende op i luften. Inde i væsken vil emulgatormolekylerne slå sig sammen i nogle klynger, der ligner kugler, og som vender de hydrofile ender ud mod vandet. En sådan sammenklumpning kaldes en micelle.
Størrelsen på miceller varierer meget, men ligger ofte på en diameter på omkring 5 mm. I en liter mælk findes ca. 2·1012 miceller.
Emulgatorer påvirker altså vandoverfladen og andre grænseflader - emulgatorer nedsætter overfladespændingen. De er overfladeaktive stoffer på samme måde som sæber eller tensider.
To slags emulsioner
En emulgator fungerer ved, at den hydrofobe del af molekylerne binder sig til upolære molekyler, samtidig med at den hydrofile kugle danner hydrogenbindinger med vandmolekyler. Små oliedråber i vand bliver endnu mindre og fordeles ensartet i væsken. Som små pigge på et pindsvin stritter de hydrofile grupper ud gennem dråbeoverfladen mod vandet og forhindrer de små dråber i at slå sig sammen til større partikler.
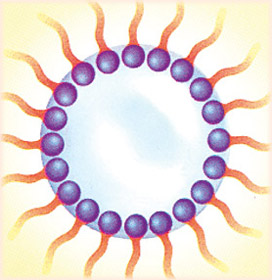
I olie-i-vand emulsioner (O/V emulsioner) er olien eller fedtstoffet fint fordelt i vand som bittesmå dråber. De holdes svævende i vandet, fordi de er indkapslet i en skal af emulgatormolekyler.
I vand-i-olie emulsioner (V/O emulsioner) er emulgatormolekylernes hydrofile kugler trængt ind i vanddråberne og vender de hydrofobe ender ud mod den omgivende olie.
 |
 |
|
Vand-i-olie |
Olie-i-vand |
Til O/V emulsioner kræves emulgatorer med relativt store hydrofile ender, fx lecithin fra æggeblomme. Monoglycerider er velegnede til V/O emulsion, som kendes fra fx margarine.
Proteiner i mælk er sammen med emulgatorer med til at stabilisere fedtdråberne i O/V emulsionen. Det skyldes de ladede grupper, der sidder på proteiner, og som binder sig til de hydrofile grupper på emulgatorerne - emulgatorerne alene klarer altså ikke denne opgave.