Sådan virker de
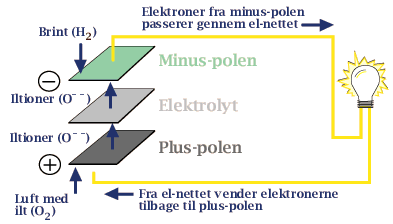
Princippet i alle brændselsceller er at få sat gang i en transport af elektroner – helt som i et almindeligt batteri. I den ene af brændselscellernes elektroder (plus-polen) sker det ved kemiske reaktioner mellem luftens ilt og elektrodematerialet, hvorved der dannes iltioner (O--), som transporteres gennem elektrolytten til minus-polen. Her reagerer iltionerne med det tilførte brændsel i form af brint, hvorved der dannes vand og frie elektroner, som derpå bliver ledt frem til »forbrugsstedet« og videre til brændselscellens plus-pol.
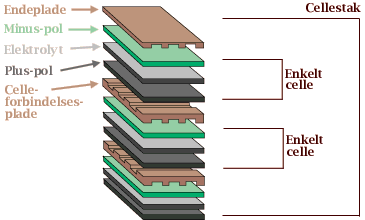
Elektrolytten
Materialet i elektrolytten består af et keramisk stof, der betegnes som yttrium-stabiliseret zirkonium-oxid (YSZ). Det er en ualmindelig god leder af iltioner. Fremstillingen af elektrolytten er en specialproces, hvor kunsten især består i at behandle keramikpulveret på den rette måde. Den færdige elektrolytplade er mindre end 0,2 mm tyk og måler 80x80 mm.
Brændselselektroden
Materialet på minus-polen er metallisk nikkel. Det har den egenskab, at molekyler fra den indblæste brint og iltionerne fra elektrolytten her kan reagere så elektronerne afgives fra brintatomerne til nikkel-metallet. Det betyder, at det er vigtigt at have en stor grænseflade mellem elektrolyt, nikkel og gas. Det forsøges opnået ved at blande YSZ og nikkel.
Luftelektroden
Også plus-polen er en blanding af YSZ og keramisk materiale. Her i form af lanthan, strontium og mangan, (LSM). Som et led i forskningsprojektet på forskningscenter Risø undersøges både egenskaberne af selve LSM-materialet og de reaktioner mellem LSM og YSZ, som omdanner ilt til iltioner.